��ҕ3��15������ǏV�����M����ه��ݛՓꇵأ�Ҳ�ǾS�o���M�ߙ���Ĵ����~������3.15���PʳƷ��ȫ��Ԓ�}����Ȼ������Pע�����c����Ҵ��ɹ����Иˡ�������ϫFˎ��������I�E�÷Ƿ����ӄ����}�������L���˼⡣

��Ҵ�������������������ù�����ǰ�େf��������������@Щ��Ƨ���ֵij��F��Ҳ�o�҂�һ���ռ�ʳƷ��ȫ֪�R�ęC������߅���ؽ�Bһ����Ҵ���
��Ҵ�����Ҵ��ַQ�����������Ʒ���鱶���Z�������`��������Ҵ����ж������@����e���ԣ�����������������@���»����ã�����Ҳ�Н��ڵ������ԣ����»��Σ���ͻ׃���°��������Ҵ��������͚W�˶�����ֹ����������ӄ����҇�2005��桶�Fˎ�䡷�Լ������ˎ�����ӄ�ʹ��Ҏ����Ҳ�����_Ҏ������Ҵ��m�÷�����35�������µ��i���������ݡ��������w�س��^35kg���i����ˎ��35�졣
�岥һ�ΏV�棺���Ϻ������z�y���g����˾������2012�꣬��һ�Ҫ����ĵ������z�z�y�C���������ԁ�һֱ��������������ИI���_չ�ˎ����w��������ИI��ȫ���z�y�Ŀ����Ҵ������ճ��O�y�^����Ŀ֮һ���Йz�y��������ѿ����c��������˾ϵ��
�V���ꮅ�������ռ�һ�z�y֪�R���o��ҽ�Bһ���������Ҵ��ęz�y������
�������Ҵ��Ĝy��
1���˜�����
���r�I��2086̖����-5-2014 ����п�������������ୡ��ϩͪ����Ҵ��Ĝy�� Һ��ɫ�V-���|�V����
2���m�÷���
���˜��m���������ϡ���s��ϡ������a���Ϻ����ӄ��A����������������������ୡ��ϩͪ����Ҵ������Ĝy�� ��
�������z�y��4�Nˎ���������Ϻ͝�s�����Йz�y���� 0. 06 mg/kg,�������� 0. 20 mg/ kg;�����a���Ϻ����ӄ��A�������Йz�y���� 0. 15 mg/kg,�������� 0. 40 mg/kg��
3������ԭ��
��������ͼ�����Һ��ȡԇ���еĿ�������������ୡ��ϩͪ����Ҵ�,�� HLB������ȡ��������Һ��ɫ�Vһ���|�V���y��,���|ƥ��˜�����У��,��˷����� ��
4���x���cԇ������
ԇ����
ɫ�V�����״������桢�������}�ᡢ���ׁ������������⛡�
6mL HLB������ȡ��
��Ҵ���Ʒ������>97.0%
�x����
Һ��ɫ�V-���|�V�x����늇��F�x��Դ��
������ƽ���x�ęC��������ȡ�b�����u���������ˮԡ������ϴ�x��0.22µm�ЙC���VĤ��
5���y�����E������Ʒ̎���^����ע��ܹ⣩
��1����Ʒ��ȡ
�ʴ_�Qȡ�����ϡ������a���Ϻ͝�s���2g�����A������1g���Լ���ͬ�|���Ļ��|ƥ��հ�ԇ�ϣ��քe��50mL�۱�ϩ�x�Ĺ��С�����0.1%����-������Һ10mL���u��1min��40�泬10min��9000r/min�x��15min���ռ�����Һ��������0.1%����-������Һ10mL�؏���ȡһ�Σ��ϲ��ɴ���ȡҺ����鿂��ȡҺ���ʴ_��ȡ5mL����ȡҺ��10mLԇ���У�60���µ��ⴵ���s2mL������0.1mol/L����������Һ4mL������ܽ⚈����������Һ��
��2����Ʒ����
ȡHLB������ȡ����������3mL�״���3mLˮ���ȡ����Һ�^����������0.02mol/L�}��3mL��5%�״���ϴ����5mL�״�ϴÓ���ռ�ϴÓҺ�����ⴵ�ɣ�����20%������Һ1mL����ܽ⣬�^0.22��m�VĤ���ϙC�y����
��3�����|ƥ���˜�����
�Qȡ6���հ���ϣ������ϲ��E�M�И�Ʒ̎�����Ƶö���1mL�հ��|��Ʒ��Һ����Ͼ��ʴ_��ȡ���m��ȵ���Ҵ��˜ʃ���Һ�����ⴵ�ɣ���1mL�հ��|��Ʒ��Һ�ܽ⣬���Ƴɝ�Ȟ�25��50��100��200��500��1000��g/mL�Ę˜ʹ���Һ���^0.22��m�VĤ���ϙC�y�����L�Ƙ˜�������
��4���y��
ɫ�V�����l����
ɫ�V����C18��,���L50 mm,�ȏ�2. 1 mm,����1. 7 µm
�����ࣺA:0.1%�����������Һ B:0.1%�����ˮ��Һ
���٣�0.2mL/min
�M���w�e��10��L
��1 �ݶ�ϴÓ����
��̖ | �r�g.min | A.% | B.% |
1 | 0 | 88 | 12 |
2 | 1.0 | 88 | 12 |
3 | 2.0 | 50 | 50 |
4 | 3.5 | l2 | 88 |
5 | 4.5 | 88 | 12 |
6 | 5.0 | 88 | 12 |
�|�V�����l����
�x��Դ��늇��F��ESI��
���跽ʽ�����x������
�z�y��ʽ���෴���O�y��MRM��
��x늉���2.8KV
Դ�أ�80��
�F���ضȣ�350��
�F�ך����٣�27L/h
�F�������٣�600L/h
��2 ���ԡ������x�Ӻ��F��늉�����ײ����
ˎ�����Q | �����x�ӌ� M/Z | �����x�ӌ� | �F��늉� | ��ײ���� |
m/ z | v | eV |
��Ҵ� | 264>143 | 264>143 | 25 | 30 |
254>212 | 25 | 30 |
(5)���Ԝy��
Ŀ��ˎ���x��1��ĸ�x�Ӻ�2�������x��,����ͬԇ�l����,��Ʒ�д��y���|�ı����r�g�c�˜���Һ�Ќ����ı����r�gƫ����12.5%֮��,�Ҙ�Ʒ�и��M�ֶ����x�ӵ������S���c��Ƚӽ��Ę˜���Һ�Ќ����Ķ����x�ӵ������S���M�б��^,ƫ����^��3Ҏ���ķ���,�t���ж����Ʒ�д��ڌ��������y�
��3 ���Դ_�C�r�����x���S�ȵ�������Sƫ��
��λ��ٷ���
�����x���S�� | >50 | >20~50 | >10~20 | ��10 |
���S�����ƫ�� | ��20 | ��25 | ��30 | ��50 |
��6�������y��
�ڃx����ѹ����l����,�����|ƥ��˜���Һ�M��,�Է���e��v���ˡ����|ƥ��˜���Һ��Ȟ�M�����L�ƹ�������,�Æ��c����cУ������Ʒ�M�ж���,��Ʒ��Һ�д��y���푑�ֵ�����ڃx���y���ľ��Է����� �� ����ɫ�V���|�V�l����,���|ƥ��˜���Һ�����f��ɫ�V�D���£�
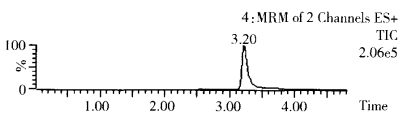
��7���Y��Ӌ��
ԇ������Ҵ�����X�����|���֔�Ӌ����λ�����ÿǧ�ˣ�mg/kg��
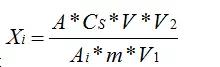
A ����ԇ����Һ�Ќ���Ŀ��ˎ��ķ���e��
As �������|ƥ��˜���Һ�Ќ���Ŀ��ˎ��ķ���e��
Cs �������|ƥ��˜���Һ�Ќ���Ŀ��ˎ��ĝ�ȣ���λ��µg/mL��
V ��������Һ�w�e����λ��mL��
M ������Ʒ���|������λ��g��
V1 ������ȡҺ�w�e����λ��mL��
V2 ��������ȡҺ�w�e����λ��mL��
�y���Y����ƽ�Мy�����㔵ƽ��ֵ��ʾ���Y��������λ��Ч���֡�


�L���Pע�������z�y�Ź���̖��